商品名称
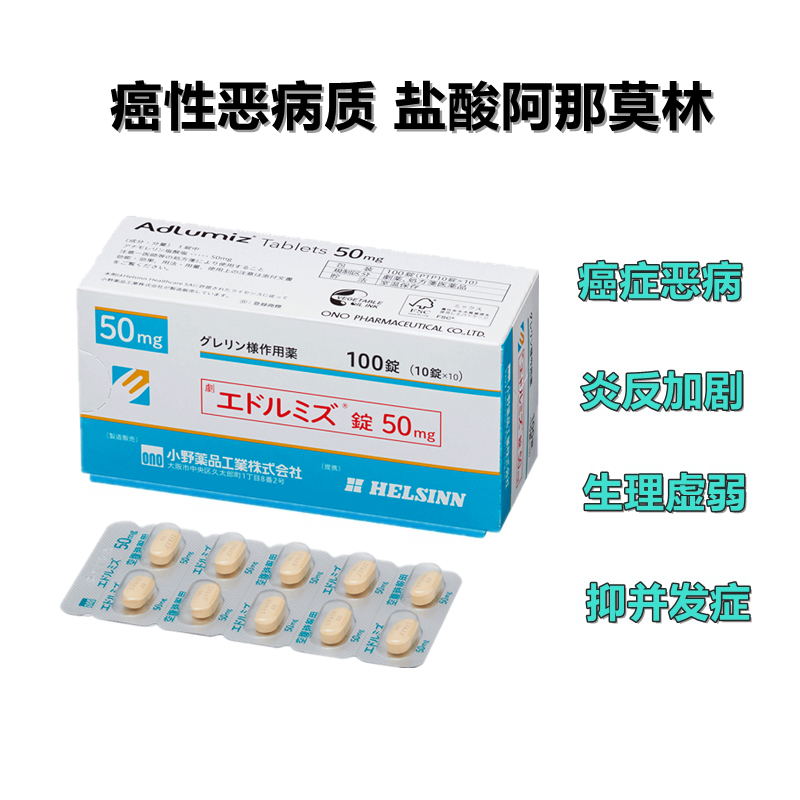
盐酸阿那莫林(Anamorelin)50mg 癌性恶病质 炎症反应加剧 生理性虚弱 抑制癌症并发症 早期介入 抗癌药物价格
¥2,304.00
48,000日元
数量
商品详情
| 日文商品名 | Adlumiz(エドルミズ錠(Anamorelin))50mg |
|---|---|
| 制造商 | 小野制药 |
| 销售商 | 小野制药 |
| GS1 | - |
| 烈性药 | - |
| 成分代码 | - |
| 内容量 | 100粒/盒 |
| 邮寄方式 | 海外直邮 |
| 限购数量 | 999 |
| 付款方式 | 1.微信/支付宝/银联,2.国际汇款,3.日本境内汇款 |
| 备货~发货所需时间 | 确认付款后,一般 5~10 个营业日左右可以发货。 |
注意
本剂应在有充分知识经验诊断和治疗癌症恶液质的医生的指导下,只给那些认为适合服用本剂的病例使用。另外,在开始使用本药剂之前,应向患者或其家属充分说明本药剂的效益和风险,在确认了解后再开始使用。
商品特征
阿那莫林,也被称为Adlumiz或エドルミズ錠,是一种由日本小野制药研发的创新型口服小分子药物。它属于胃动力药的一种,通过激活胃饥饿素受体,模拟胃肠道自然分泌的胃饥饿素,刺激食欲、促进食物摄入和吸收,从而有效改善癌症恶病质患者的营养状况。这种药物于2021年4月在日本上市,并迅速成为治疗非小细胞肺癌、胃癌、胰腺癌、结直肠癌等恶性肿瘤患者恶病质的重要选择。
规格
100粒/盒
形状
片剂
成分说明
盐酸阿那莫林
功能主治
用于治疗非小细胞肺癌、胃癌、胰腺癌、结直肠癌等恶性肿瘤患者的癌症恶病质。
1 .应用于不能切除的进展复发的非小细胞肺癌、胃癌、胰腺癌、大肠癌的癌变液质患者。
2 .用于营养疗法等效果不充分的癌症恶液质患者。
3 .用于6个月内有5%以上体重减少和食欲不振,且有以下(1)、(3)中2个以上的患者。
(1)疲劳或疲劳感。
(2)全身肌力下降。
(3)CRP值超过0.5mg/dL、血红蛋白值小于12g/dL或白蛋白值小于3.2g/dL中任意一个以上。
4 .请勿用于饮食口服摄入困难或饮食消化吸收不良的患者。
5 .要熟悉“临床成绩”项的内容,在充分了解临床试验对象的患者背景、本剂的有效性和安全性的基础上,进行适应患者的选择。
(参考)(1)疲劳或疲劳感,(2)全身肌力下降,参考NCI common terminology criteria for adverse events ( CTCAE)日语版JCOG翻译进行评价,以Grade1以上为症状标准。另外,关于肌力下降,也要参考握力、步行速度、椅子站立等指标进行评价。
用法用量
通常,成人每天1次空腹口服100mg作为肾上腺素盐酸盐。
1 .为避免饮食影响,本剂应在空腹服用,服用本剂后1小时内不进食。(参见“药物动力学”一项)
2 .如果因服用本剂而未发现体重增加或食欲改善,原则上应在开始服用3周后停止服用。
3 .没有服用本剂超过12周的经验,应定期探讨通过体重、问诊确认食欲等继续服用的必要性。(参照“临床成绩”一项)
注意事项
慎重给药,对以下患者要慎重给药:
1 .有基础心脏病(瓣膜病、心肌病等)的患者〔抑制心功能,症状有可能恶化。〕
2 .既往有心肌梗塞或心绞痛的患者〔抑制心功能,症状有可能恶化。〕
3 .有刺激传导系统障碍(房室传导阻滞、窦房结、脚阻滞等)的患者(本剂具有钠通道抑制作用,因此有抑制性作用于刺激传导系统,恶化的危险。〕(参见“重要的基本注意事项”、“重大副作用”一项)
4 .有延长Qt间隔或既往有Qt间隔史的患者〔有延长Qt间隔的危险。〕(参见“重要的基本注意事项”、“重大副作用”一项)
5 .有电解质异常(低钾血症、低镁血症、低钙血症)的患者〔可能出现刺激传导系统抑制〕。〕(参见“重要的基本注意事项”、“重大副作用”一项)
6 .有使用四环素类药物经历的患者
7 .有轻度肝功能损害( Child-Pugh分类a )的患者。有轻度肝功能障碍的患者合并使用中度CYP3A4抑制剂时,要特别注意。〔由于肝脏主要帮助本剂从体内消失,因此血药浓度上升,可能出现刺激传导系统抑制。另外,如果并用中度的CYP3A4抑制剂,有可能阻碍本剂的代谢,进而导致血药浓度上升。〕(参见“相互作用”、“重大副作用”、“药物动力学”一项)
8 .糖尿病患者〔有时会导致血糖值上升。〕
禁忌
【重要基本注意事项】
1 .本剂具有钠通道抑制作用,因此对刺激传导系统有抑制作用。由于给药时会出现心电图异常(明显的PR间隔或QRS宽度延长、QT间隔延长等),因此在给药开始前及给药期间,应定期测量心电图、脉搏、血压、心胸比、电解质等,如发现异常,应停止给药 另外,在给药初期要特别注意。(见“严重不良反应”、“临床成绩”一项)
2 .由于有时会出现高血糖,因此在本剂给药开始前及给药期间应定期进行血糖值和尿糖的测定。(见“严重不良反应”一项)
3 .由于有时会出现肝功能障碍,因此在本剂开始给药前及给药期间应定期进行肝功能检查。(见“严重不良反应”一项)
【相互作用】
本剂主要由CYP3A4代谢。(参见“药物动力学”一项)
【副作用】
在日本国内第II相试验和第III相试验( ONO-7643-03、04和05试验)的安全性评价对象187例中,有84例( 44.9% )发现了副作用(包括临床检查值异常)。主要副作用为γ-GTP增加12例( 6.4% ),糖化血红蛋白增加11例( 5.9% )。(批准时)
严重不良反应:
1 .刺激传导系统抑制( 10.7% )心电图异常(明显的PR间隔或QRS宽度延长、QT延长等),有时会出现房室传导阻滞、心动过速、心动过缓、心悸、血压下降、上室性期外收缩等,因此在发现异常时停止给药
2 .高血糖( 4.3% )、糖尿病恶化( 4.3% )高血糖、糖尿病恶化,应注意口渴、尿频等症状的表现,必要时停止服用胰岛素、口服降糖药和本剂等妥善处理。
3 .肝功能障碍( 6.4% )由于有时会出现伴随AST、ALT、ALP、γ-GTP、血中胆红素等上升的肝功能障碍,因此在发现异常的情况下,应停止给药等适当的处理。
【特殊人群用药】
给老年人的用药
一般来说,老年人的生理功能(肾功能、肝功能、免疫功能等)下降,因此,要一边观察患者的状态,一边慎重服用。
给孕妇、产妇、哺乳妇等用药
1 .对于孕妇或有可能怀孕的女性,仅在判断为治疗上的有益性超过危险性时给药。〔通过给小鼠注射饥饿激素或饥饿激素模拟,发现胚胎发生延迟、胎儿体重低值、妊娠率下降、胎儿数减少。1,2 )另外,虽然不清楚本剂的胎盘通过性,但考虑到脂溶性高、弱碱性等,有通过胎盘的可能性。〕
2 .考虑哺乳妇女在治疗上的有益性和母乳营养的有益性,考虑继续或停止哺乳。〔本剂向乳汁中的转移尚不清楚,但考虑到脂溶性高、弱碱性等,有可能向乳汁中转移。〕
给儿童等的给药
没有对儿童进行临床试验。
※ 详细请参考说明书: 「添付文書情報」 点此输入日文商品名可查询日文原版说明书
商品评价
-
